化学漫谈004
很久没写这个系列了,我计划重新把这个系列捡起来,主要写一些反应在合成中的应用以及天然产物全合成的内容,这一篇就先从天然产物介绍开始吧。
简述
天然产物(Natural product)顾名思义就是自然界中本身就有的化合物,或是指那些由有机体产生的物质,天然产物这一概念无疑是和生物联系非常紧密的[1]。
But what is ‘natural’? The simplest definition for a natural product is a small molecule that is produced by a biological source.
当然这是相当广泛的定义,但是也可以从侧面映照出天然产物其实是与我们的日常生活关系非常紧密的,它们的数量也非常的多,根据数据显示,我们已知的天然产物可能在30万种到40万种之间[2]。
有机领域关心的天然产物大多是生物的初级代谢产物或次级代谢产物(小分子化合物),也因此许多天然产物都具有细胞毒性/生物活性/药物价值。天然产物和衍生物为新药研发提供了重要的参考,在每年批准的新药中都占有一定份额。
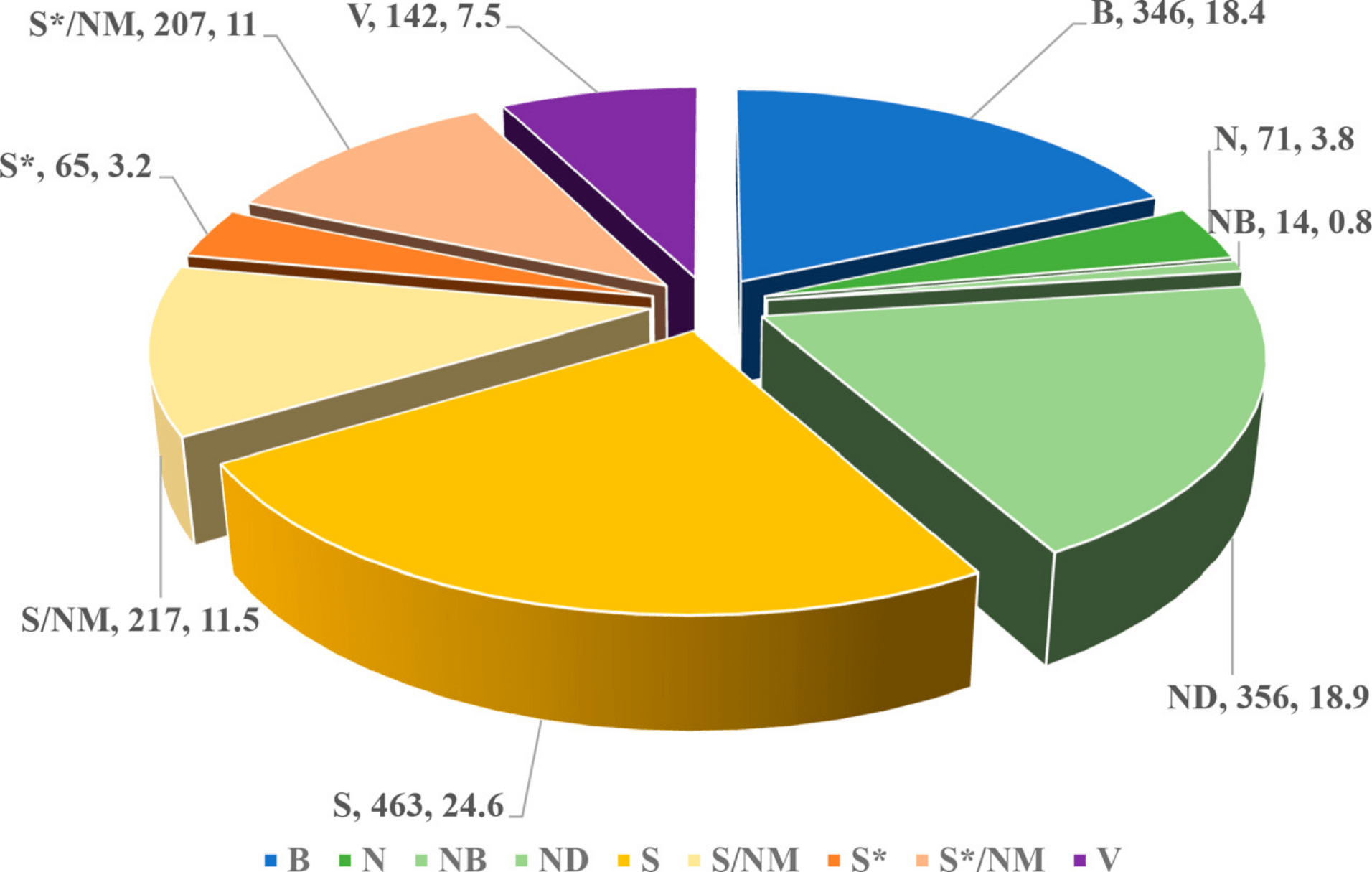
上图中为从1981年1月1日到2019年9月30日止的所有批准药物分类记录[3],其中 N 指未修饰的天然产物,NB 指天然产物植物制剂,ND 指天然产物衍生物,如果再算上 B(生物大分子)和 NM(天然产物仿制物)就更多了。可见天然产物研究在这39年的药物研发中发挥的重要的作用。
经典的几个例子如:Artemisinin (即青蒿素,是目前治疗恶性疟原虫疟疾起效最快的药物)、Rotenone (鱼藤酮,是一种广泛使用的植物来源杀虫剂)、Paclitaxel (大名鼎鼎的抗癌药物紫杉醇)、Doxorubicin (即阿霉素,用于治疗癌症)等。
来源分类
天然产物可以从微生物、植物和动物的细胞、组织和分泌物中提取而来,粗提取物往往是多种化合物的混合,还需要进一步的筛选、生物检定、分离纯化才能得到纯的具有生物活性的天然产物。
下面按照来源的不同对各类型天然产物分类介绍:
细菌来源
从微生物中尝试提取天然产物要追溯到盘尼西林的发现和广泛应用,在那之后,人们开始关注这些之前总被忽视的微小生物,并展开大规模的搜寻以便发现更多的可应用的抗感染用途天然产物。
比如 Streptomycin (链霉素),由 Albert Schatz 于1943年发现,当时他正在 Rutgers 大学 Selman Abraham Waksman 教授课题组当博士生[4]。Streptomycin 是第一个被发现能够有效治疗结核病的抗生素。由于链霉素用于治疗结核病的良好效果,1952年的诺贝尔生理学或医学奖被授予给了 Selman Abraham Waksman。
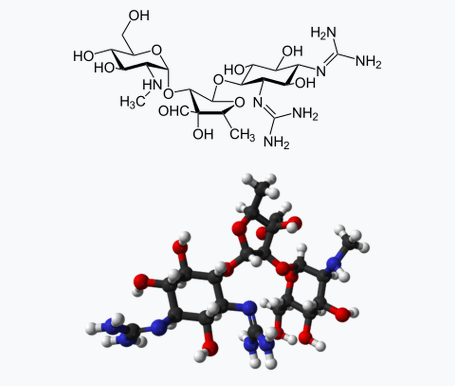
( 你可能会想为什么 Schatz 发现了链霉素,诺奖却给了导师 Waksman。事实上的确有人提出了质疑,在奖项颁布后,有人指控 Waksman 强占了 Schatz 的研究成果,并且 Elizabeth Bugie (她是 Waksman 实验室的一名硕士) 实际上在链霉素的发展过程中起了更大的作用[6]。最后,这场风波以 Schatz 获得了 Waksman 的奖金的30%收尾,而 Bugie 仅获得了奖金的2%。 )
这个重要药物的发现让人们意识到细菌可能是药物活性天然产物的重要来源之一[7],因此引发了许多抗菌和抗真菌药物的迅速发展,如 amphotericin B(两性霉素 B), chloramphenicol(氯霉素), daptomycin(达托霉素), tetracycline(四环素), polymyxins(多黏菌素) 等等。
上述的各种药物都是抗感染药物,但其实细菌来源的天然产物在各个领域都有用武之地:
Botulinum toxin(也称 botox,肉毒杆菌毒素)是从 Clostridium botulinum 和相关物种中提取出的一种神经毒性蛋白质,它毒性极强,是人类目前已知的最强毒素之一($LD_{50}=1.3\sim2.1\ ng/kg$),但是极低剂量注射于特定肌肉位置时可以治疗肌肉痉挛,同时还能消除皱纹,因此也被用于美容手术。
Pingyangmycin(平阳霉素,也称 bleomycin $A_5$),顾名思义,它是在中国浙江省平阳县发现的,属于 bleomycin 家族中的一员,从当地的 Streptomycin verticillus var. pingyangensis n.sp 变种中获得,具有很好的抗癌活性,且相对于 bleomycin $A_2$ 更便宜、有效,对多种癌症都有效果[8]。
一些在极端条件中生存的古生菌(Archaea)体内的酶往往具有常规条件下不具备的神奇特性,不过这一部分不在本文讨论的范围内,此处略去。
真菌来源
最出名的一个例子无疑是 Penicillin (盘尼西林),Penicillin 由苏格兰医生 Alexander Fleming 于1928年从 P. rubens 的粗提取物中发现[9]。其纯化的化合物 (penicillin F)由牛津大学的 Howard Florey 和 Ernst Boris Chain 研究团队分离得到,后来他们三人共享了1945年的诺贝尔生理学或医学奖。penicillin 已经成为最广泛应用的抗感染药物之一。
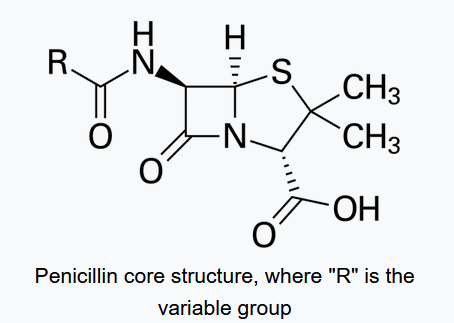
再如 cephalosporins (头孢菌素),从霉菌 Cephalosporium acremonium 中提取出来,可用于预防和治疗多种细菌感染;Griseofulvin (灰黄霉素)是一种用于治疗脚气的抗真菌药物,于1939年从土壤真菌 Penicillium griseofulvum 中被发现。
当然,除了抗感染,真菌中提取出的产物也有很多其他的功能。Lovastatin (洛伐他汀)最早于1970年前后在 Pleurotus ostreatus 中发现,具有治疗高血胆固醇和降低心脑血管疾病风险的功效,于1987年正式被批准药物应用[10]。
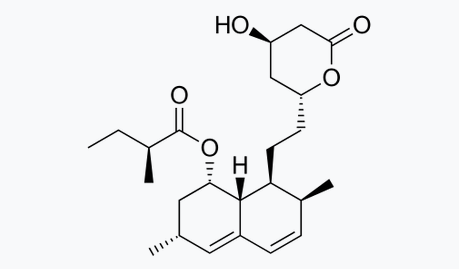
Ergonovine (麦角新碱,也称为 lysergic acid propanolamide,即麦角酸酰胺)在1932年从 Claviceps 中获得,用于治疗重症产后出血;Cyclosporin (环孢素)是一种从 Tolypocladium inflatum 中获得的免疫抑制剂,可治疗类风湿关节炎、牛皮藓、克罗恩病等,在1983年进入临床应用[11]。
植物来源
植物是各种结构复杂且多样化的天然产物的主要来源,这可能是因为植物在长期的进化中需要合成各种有毒物质来抵御食草动物和病原体的攻击[12],也恰恰是这些毒性物质,蕴含着作为农药或医疗药物的潜在可能。
首先是抗癌“明星分子” Paclitaxel (紫杉醇,商品名 Taxol),能够治疗多种癌症,如食道癌、乳腺癌、肺癌等。Paclitaxel 最早于1971年中从太平洋紫衫(Taxus brevifolia)中被分离出来,并于1993年被批准作为药物使用[13]。
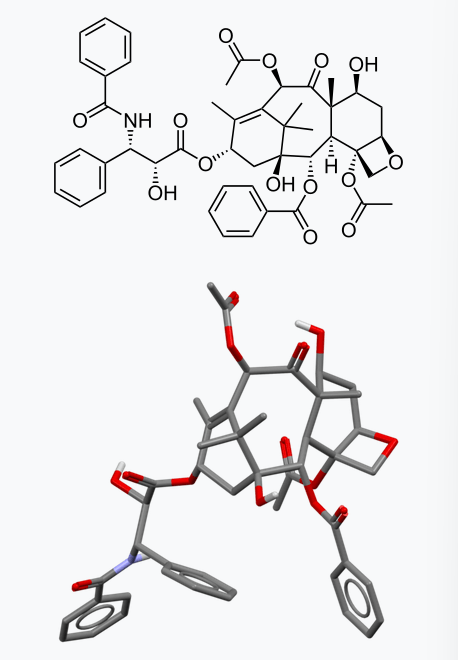
在1993年以前,几乎所有的 Paclitaxel 都是从太平洋紫衫的树皮中获得,紫衫树被剥去树皮后就会死亡,所以很显然这种提取方式难以为继,而且树皮中的 Paclitaxel 含量极低,即使收集了大量紫衫树皮也很难满足需求。人们开始尝试从紫衫针叶中提取,或者开始人工种植太平洋紫衫及相关物种,但是这些举措仍然没有从根本上解决问题。
一些化学家们注意到了这一问题,开始着手于 Paclitaxel 的人工合成策略。其中弗罗里达州立大学的 Robert A. Holton 教授团队在1989年开发出了 paclitaxel 的一种半合成策略[14],并和 Bristol-Myers Squibb (BMS)公司达成合作,许可其使用 Holton 教授的策略制造 paclitaxel。
1992年,Holton 教授将半合成产率优化至80%,同时 BMS 公司开始使用欧洲紫衫的针叶中分离出的原料大规模制造 paclitaxel。2013年,另一家公司 Phyton Biotech 开始使用植物细胞发酵(PCF)技术制造 paclitaxel,相比于半合成方法又有所进步,不需要使用紫衫原料,直接培养特定的细胞,让细胞生成产物[15]。并且这种方法易于富集得到高纯度的 paclitaxel,也不需要用到半合成方法中的许多有毒有害试剂,目前仍是主流的制备方案之一。
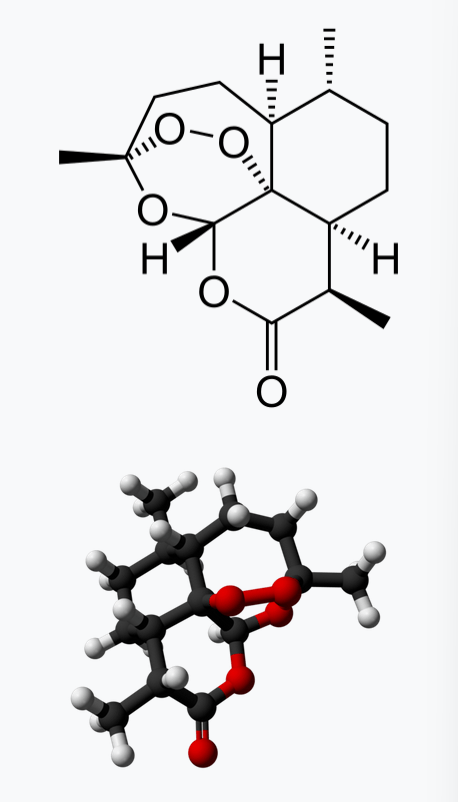
再比如 Artemisinin (青蒿素),于1972年被屠呦呦从 Artemisia annua 中提取出来,是治疗疟疾的有效药物,屠呦呦也因为这一发现获得了2015年的诺贝尔生理学或医学奖。
Vinblastine (长春碱,商品名 Velban)最初从 Catharanthus roseus 中分离出来,可用于治疗多种癌症。
( 长春碱从长春花中提取而得,不过这个“长春花”里的“长春”并不是指地名长春,而是指长春花花期长,经久不凋。在清代吴其濬所著《植物名实图考》中记载:
长春花\桑华叶\如精显先匿六月中园\五盐小紫花\背白遂盐发小茎\园花极盐\结长角\有园圈于围\秋至冬园放\不图不经显\霆不妻\故名
另有宋代女诗人朱淑真所作七言绝句《长春花》:
一枝才谢一枝殷,自是春工不与闲。
纵使牡丹称绝艳,到头荣瘁片时间。
)
还有许多植物衍生出的药物,例如 morphine (吗啡)、cocaine (可卡因)、quinine (奎宁)等等。
动物来源
动物也是一个重要的生物活性天然产物的来源,和植物类似,许多有毒性的动物(例如蛇类、蜘蛛、蜜蜂、蝎子、青蛙等等)格外受到化学家们的关注。它们体内的毒素往往可以和捕食者体内的大分子受体发生相互作用,以此来保护自己免受捕食者的伤害。
这些毒性物质大多会影响捕食者的神经区域,导致其瘫痪/死亡等,因此是研究受体/离子通道/酶作用机制的重要工具。
Teprotide (替普罗肽)是从蛇类 Bothrops jararaca 的毒液中分离出来的一种九肽,是一种血管紧张素转化酶抑制剂(ACE inhibitor),即可以抑制这种转化酶的活性,使血管无法收缩紧张,可以作为降压剂。它的发现和机理研究带动了相关抗高血压药物(普利类)的发展,例如 Cilazapril (西拉普利)和 Captopril (卡托普利)。
Echistatin (锯鳞肽)是从蛇类 Echis carinatus 中分离出来的一种解聚素(disintegrin),它会和凝血蛋白受体结合,阻碍凝血过程,使伤口血流不止。它的这种毒性促进了抗血小板聚集药物的研发,例如 tirofiban (替罗非班)[16],可用于防止血栓形成和进一步扩大。
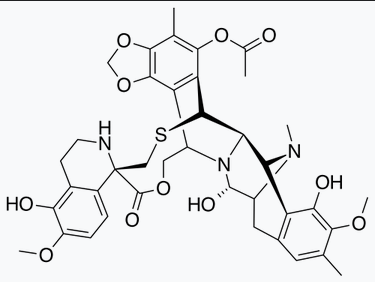
许多海洋生物具有非凡的能力,其代谢物具有非常好的生物活性。例如 ecteinascidin 743 (又称 trabectedin,即曲贝替定)从一种海鞘 Ecteinascidia turbinata 中被发现,后由 KL Rinehart 教授在1984年测定了结构[17]。Trabectedin 可以用于治疗晚期软组织肉瘤和卵巢癌。
结构分类
天然产物家族非常庞大,但是根据结构不同(或者说是生源合成的方式不同)可以粗略的分为几个大类[18],下面逐一介绍。
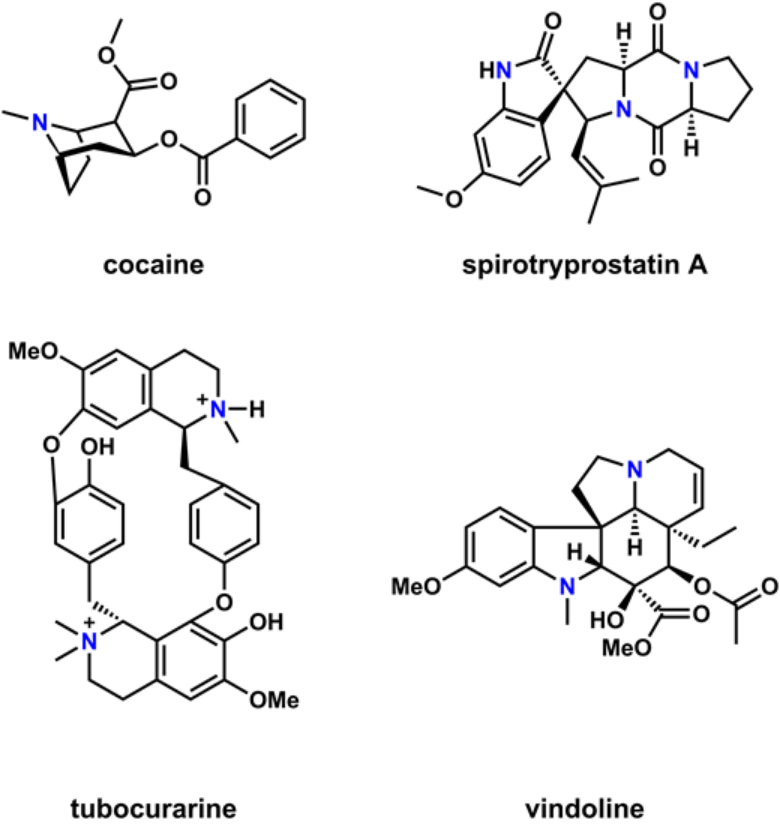
Alkaloids 生物碱类
生物碱类的包含范围较广,只要分子中存在能够质子化的含氮基团就可以归入此类,因为含氮基团为碱性而得名。
由于生物碱的定义对骨架没有要求,所以不同生物碱分子的结构可能差别巨大。再进一步细分,可以把生物碱类分为氨基酸来源和吲哚萜烯(indole terpene)骨架两类。
Peptide-based 多肽类
多肽类天然产物主要来源于蛋白质的选择性水解和蛋白质前体的修饰。
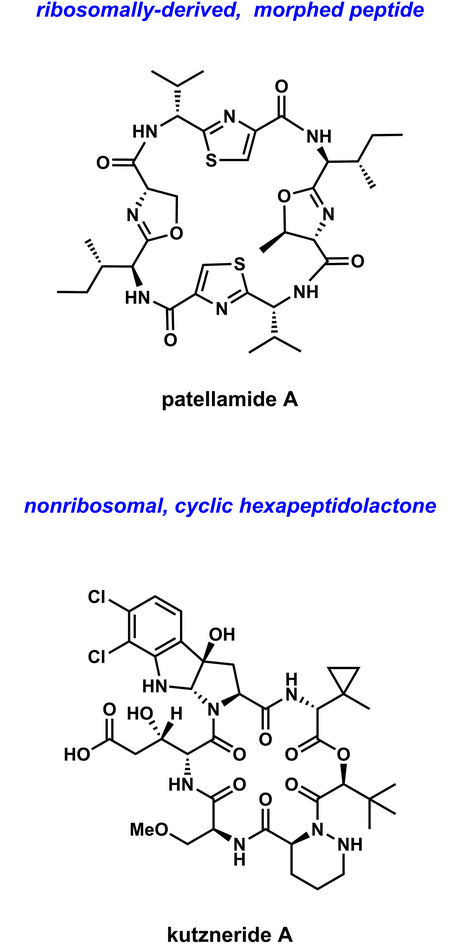
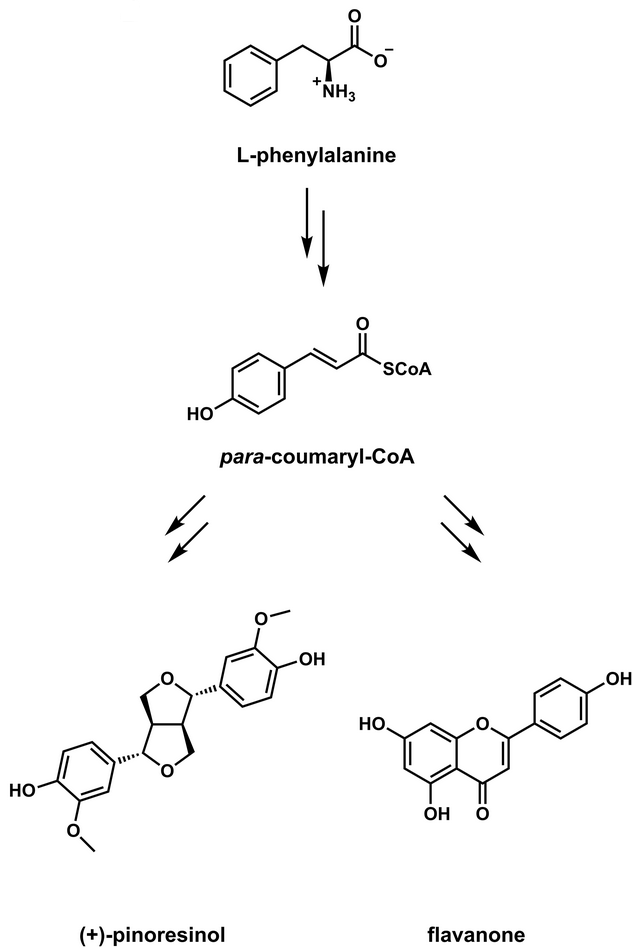
Phenylpropanoid 苯丙素类
苯丙素类天然产物多见于植物代谢产物,由九个碳的 phenylalanine (苯基丙氨酸)经历代谢转化而来。
Terpenoids 萜烯类
萜烯类,也被称为 isoprenoids (类异戊二烯),是最大的一类天然产物分类,存在超过50000种萜类化合物。这些化合物的一个共同点就是具有由若干个五碳的异戊二烯结合成的骨架。
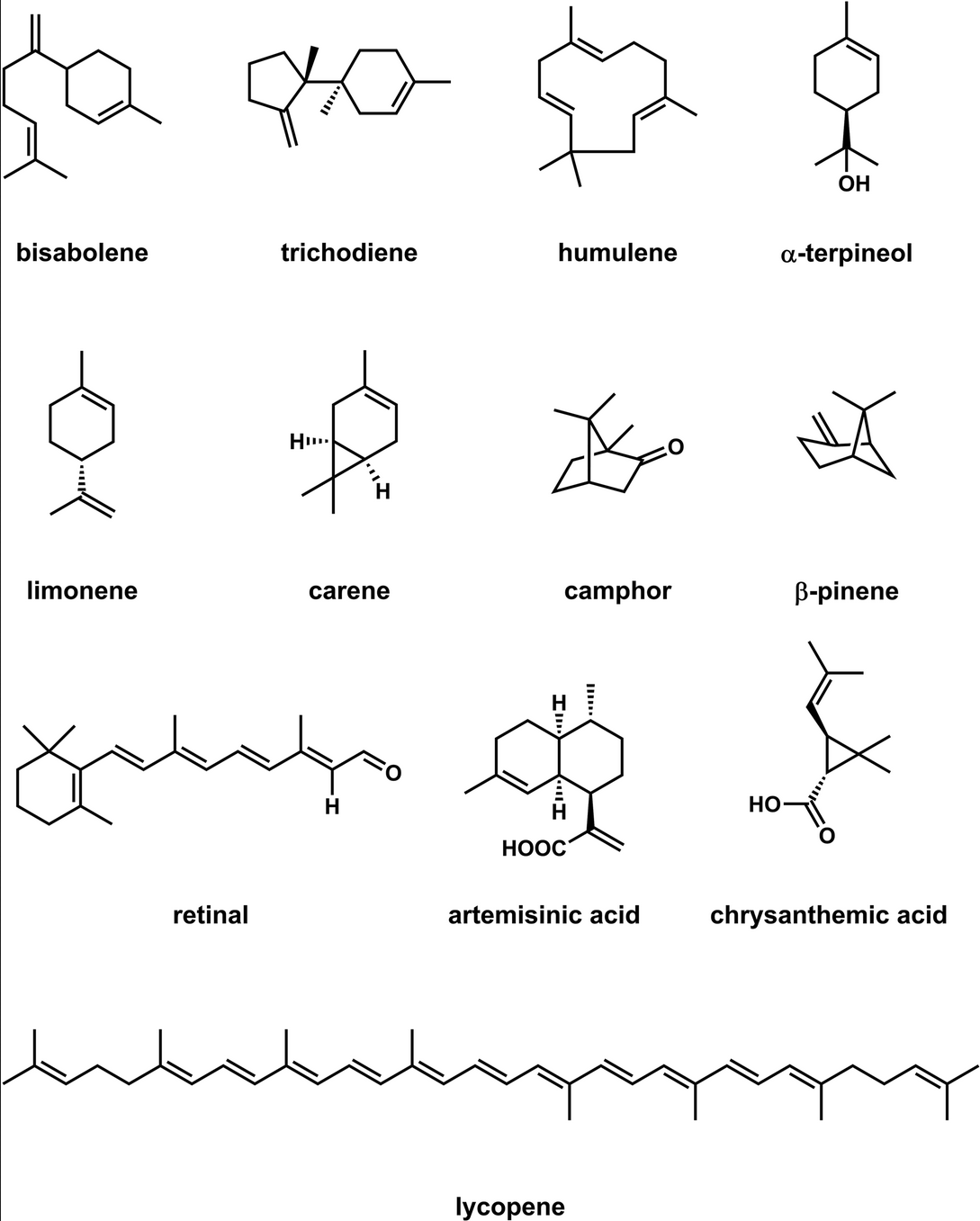
按照异戊二烯单元的数量,可以分为半萜(一个异戊二烯单元,5个碳)、单萜(两个异戊二烯单元,10个碳)、倍半萜(三个异戊二烯单元,15个碳)、二萜(四个异戊二烯单元,20个碳),以此类推。
Polyketides 聚酮类
聚酮类也是一类重要的天然产物,由一连串的羰基和亚甲基交替排列而成。在生物合成时,则是从丙二酰硫酯或甲基丙二酰硫酯不断延长碳链而得。
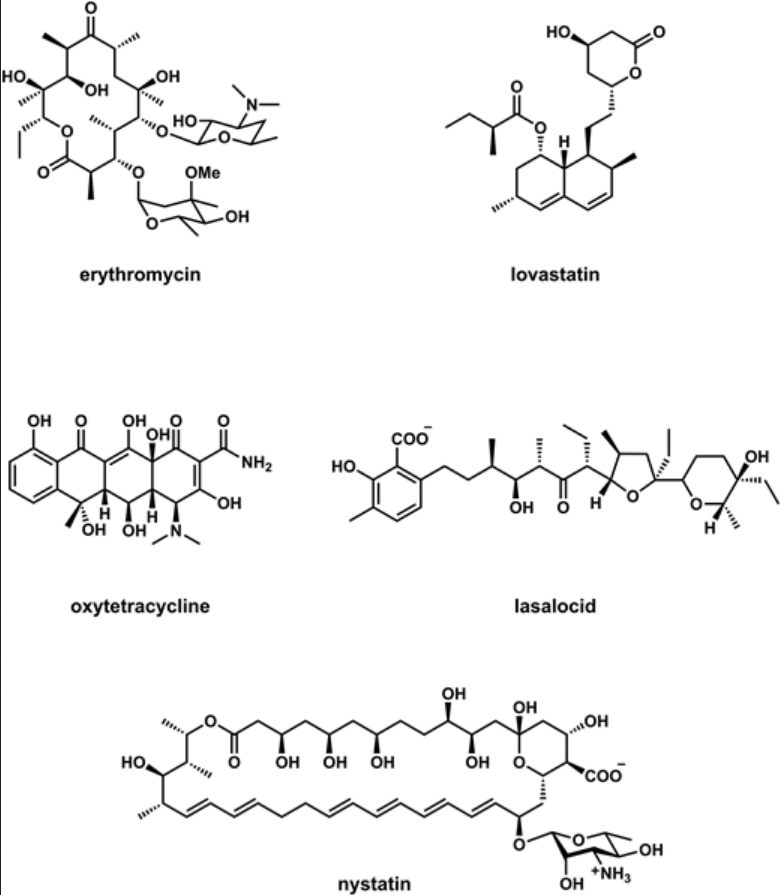
如上图所示,聚酮类可以进一步分成多个小类别,如线性的并环类(oxytetracycline)、大环内酯类(erythromycin)、含十碳萘环类(lovastatin)、多烯类(nystatin)和由多烯转化的四氢呋喃/四氢吡喃类(lasalocid)等等。
Glycosides 糖苷类
严格上这类化合物在结构上并不是独立的,而是具有糖苷基团修饰的化合物。糖苷基团可以转移到各种亲核试剂上,因此其范围非常广。它的一个重要作用是在诸多的亲水性天然产物中引入疏水基团,以平衡亲水/疏水的作用。
其例子可参考上图(图12)中的 erythromycin 和 nystatin。
机遇与挑战
从1828年维勒人工合成尿素以来,有机化学和全合成在这200年间飞速发展着。最近100年来与有机合成相关的诺奖就有28项之多,新的合成方法学、合成路线和复杂分子的合成不断涌现。不夸张的讲,人类现在已经具备合成几乎任何分子的能力,并能够将它们用于经济、健康、生活领域之中。
但是挑战同样存在着,甚至比以往更加严峻,尤其是对于有机合成这样一个灵感(serendipity)相当重要的领域[19]。首先就是人工合成和自然合成相比,在效率和精准方面仍存在差距。其次是稀缺原料逐渐减少和对可持续性的担忧对绿色化学、绿色合成提出了更高要求。
为了更好的服务人类,充分发挥化学合成的能力,它需要和其他学科与领域结合起来,作为强有力的工具发挥作用,帮助生物、物理、医药、生物技术、纳米技术等等领域拓宽探索的前沿和边界。
If the innovation and impact of organic synthesis on society in the last century is a measure of things to come, we are in for a new wave of influential discoveries and inventions. How well they will serve humanity and the planet will depend on how wisely we use them.
—— K C Nicolaou
参考
- 1.All natural. Nat Chem Biol 3, 351 (2007) ↩
- 2.Sorokina, M., Steinbeck, C. Review on natural products databases: where to find data in 2020. J Cheminform 12, 20 (2020) ↩
- 3.J. Nat. Prod. 2020, 83, 3, 770–803 ↩
- 4.Comroe JH Jr. Pay dirt: the story of streptomycin. Part I. From Waksman to Waksman. Am Rev Respir Dis. 1978 Apr;117(4):773-81 ↩
- 5.Wainwright M. Streptomycin: discovery and resultant controversy. Hist Philos Life Sci. 1991;13(1):97-124 ↩
- 6.Pringle P (2012). Experiment Eleven: Dark Secrets Behind the Discovery of a Wonder Drug. New York: Walker & Company ↩
- 7.Zaffiri, L., Gardner, J., & Toledo-Pereyra, L. H. (2012). History of Antibiotics. From Salvarsan to Cephalosporins. Journal of Investigative Surgery, 25 (2), 67–77 ↩
- 8.Lin FT, Li DD, Yang XP, Li Q, Xue YC, Zhen YS. [Antitumor activity and preclinical pharmacologic evaluation of pingyangmycin (author's transl)]. Zhonghua Zhong Liu Za Zhi. 1979;1(3):161-6. Chinese ↩
- 9.Lalchhandama K (2020). "Reappraising Fleming's snot and mould". Science Vision. 20 (1): 29–42 ↩
- 10.Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 472 ↩
- 11.Watts R, Clunie G, Hall F, Marshall T (2009). Rheumatology. Oxford University Press. p. 558 ↩
- 12.Dang L, Van Damme EJ (September 2015). "Toxic proteins in plants". Phytochemistry. 117: 51–64 ↩
- 13.Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 512 ↩
- 14.Holton RA, Biediger RJ, Boatman PD (1999). "Semisynthesis of taxol and taxotere". In Suffness M (ed.). Taxol: Science and Applications . Boca Raton: CRC press. pp. 97–121 ↩
- 15.Imseng N, Schillberg S, Schürch C, Schmid D, Schütte K, Gorr G, et al. (2014). "Suspension Culture of Plant Cells under Heterotrophic Conditions". In Meyer HP, Schmidhalter D (eds.). Industrial Scale Suspension Culture of Living Cells. Wiley-Blackwell. pp. 224–257 ↩
- 16.Lazarovici P, Marcinkiewicz C, Lelkes PI (May 2019). "From Snake Venom's Disintegrins and C-Type Lectins to Anti-Platelet Drugs". Toxins. 11 (5) 303 ↩
- 17.Rinehart KL (January 2000). "Antitumor compounds from tunicates". Medicinal Research Reviews. 20 (1): 1–27 ↩
- 18.Natural Product Biosynthesis, The Royal Society of Chemistry, 2022, ch. 1, pp. 1-21 ↩
- 19.Nicolaou KC. Inspirations, discoveries, and future perspectives in total synthesis. J Org Chem. 2009 Feb 6;74(3):951-72 ↩